Em 2019, a icônica tabela periódica completa seu 150º aniversário!
Justamente em 1869 que o químico russo Dmitry Mendeleev apresentou a tabela periódica dos elementos químicos, naquela que foi um dos mais importantes marcos da química.
Até metade de 1800, várias tentativas foram realizadas para organizar os “apenas” 63 elementos químicos que eram conhecidos até então.
Várias argumentações e lógicas foram levantadas e propostas para tal.
Os principais proponentes para esta organização dos elementos foram Johann Doebereiner em 1829, Alexander Chancourtois em 1862, Julius Meyer em 1864 e John Newlands (1866).

A partir de seus trabalhos na Universidade de São Petersburgo, durante o ano de 1867, Dmitry Mendeleev percebeu que as propriedades dos elementos e suas massas atômicas se relacionavam.
Mendeleev trabalhou na criação de grupos e períodos, posicionamento dos elementos, correções de massa de alguns deles – além de ter previsto a existência e as propriedades de elementos que ainda não eram conhecidos.
Dois anos depois, a tabela concebida por ele, chamada de O Experimento de um Sistema de Elementos Baseado em seus Pesos Atômicos e Similaridade Química, foi enviada para seus colegas na Rússia e fora dela.
Mendeleev propunha que “os elementos, se organizados de acordo com seus pesos atômicos, exibem uma aparente periodicidade de propriedades”.
Até a metade de 2019, a Tabela Periódica lista 118 elementos, e ainda há esforços para reorganizar a Tabela e isso também vamos ver hoje!
A Torre
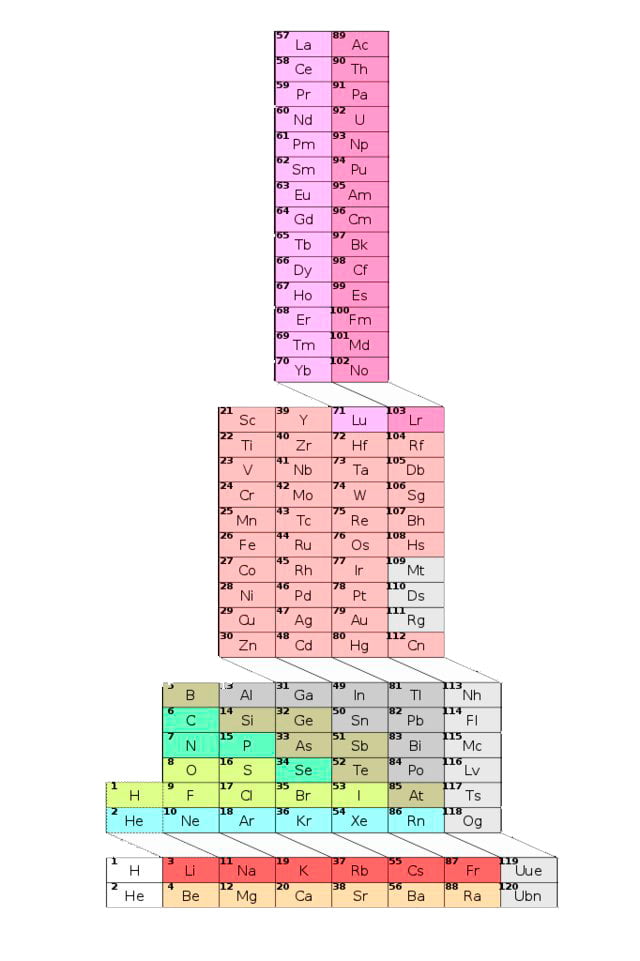
Esta tabela foi proposta por Valery Tsimmerman em 2006 e ao invés de se basear no número atômico, esta é montada considerando os quatro números quânticos da configuração eletrônica dos átomos.
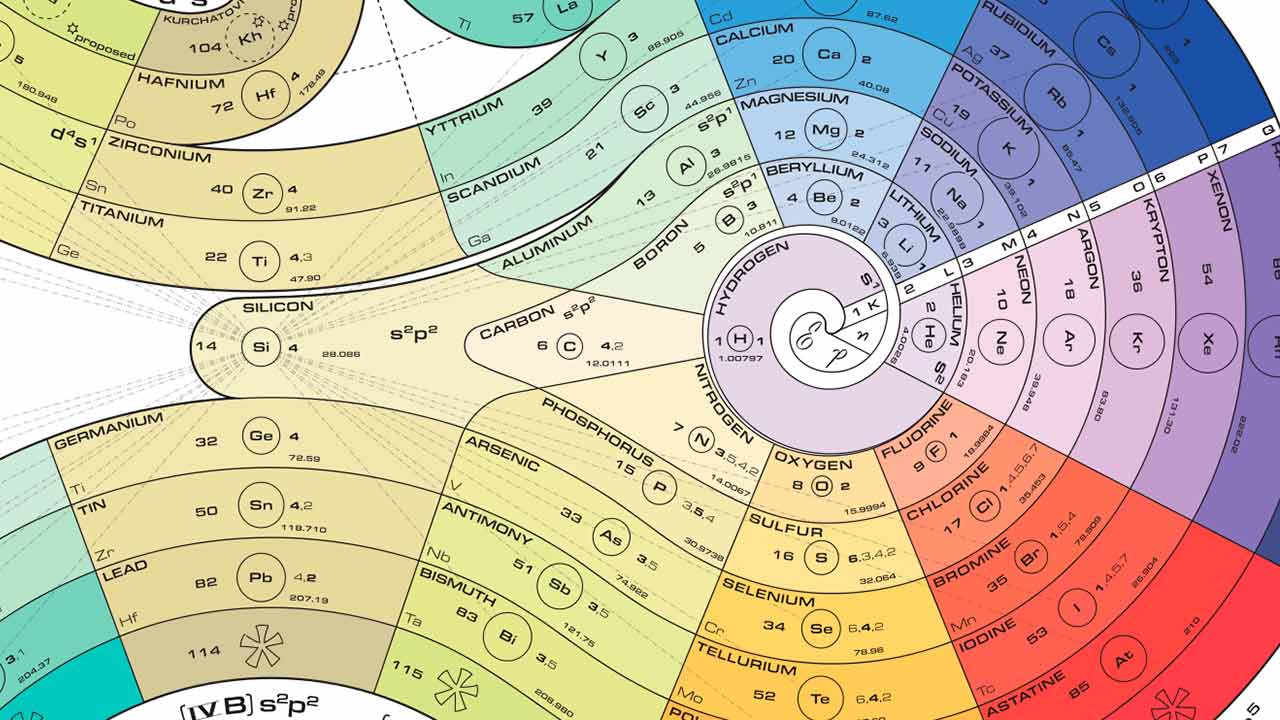
O Espiral

Esta tabela espiralada foi proposta pelo químico Theodor Benfey em 1964. Ela começa no interior do espiral e vai se desenrolando com base no número atômico.
A 3D

Nesta tabela, não está incluso o hidrogênio. A parte esverdeada corresponde aos metais alcalinos e alcalinos terrosos (orbital s), a parte azulada os não-metais (orbital p) e nas outras duas os elementos de transição (orbitais d e f).
O Laço
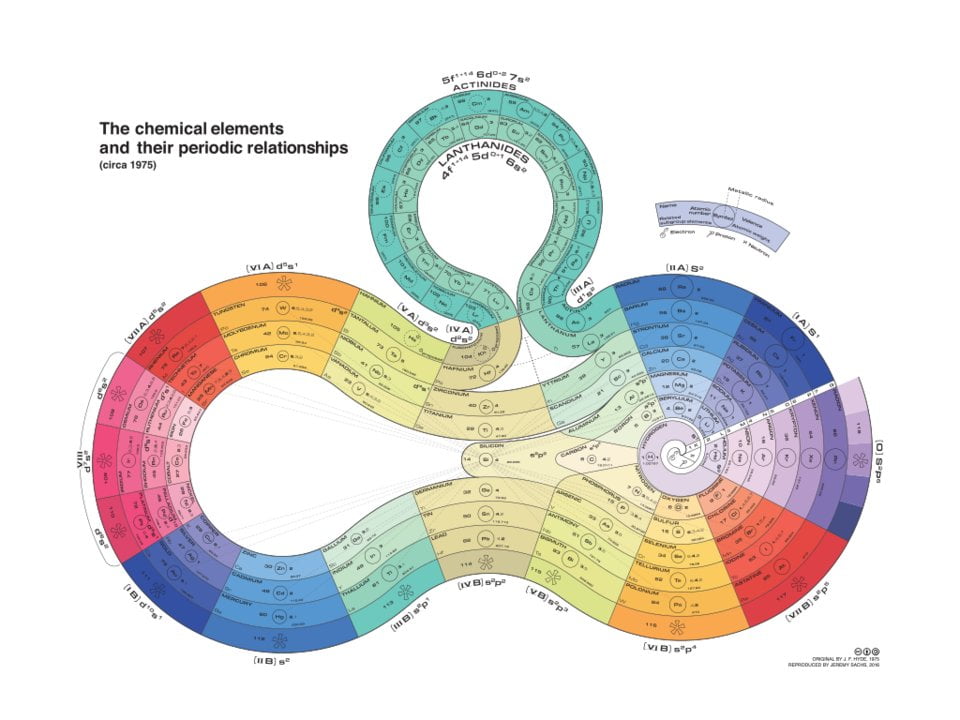
Esta tabela foi proposta em 1975, por James Franklin Hyde. Nela vemos que os elementos consecutivos estão ligados e a sequência segue um espiral fazendo alguns loops.
As cores próximas nos mostram como há uma tendência nas propriedades dos elementos. Também podemos visualizar os orbitais de distribuição eletrônica ao longo da tabela.
Fontes
There’s more than one periodic table. Here are some designs you’ve never soon
Mendeleev’s Periodic Table of Elements celebrates its 150th anniversary